|
La necessità di comprendere le concatenazioni causali su cui si fonda lo sviluppo delle
dipendenze sta alla base di ogni intervento razionale nel campo della terapia e della prevenzione, con una interpretazione dei fenomeni a partire da un attento
ascolto delle sofferenze umane dei pazienti e delle loro famiglie (Frances, 1997). Se ci si avventura nell'analisi anamnestica dell'evoluzione dei pazienti tossicodipendenti,
sin dalla loro prima infanzia e dalla familiarità, ci si troverà di fronte a quell'intreccio di cofattori, di "ferite" psicobiologiche che hanno determinato la vulnerabilità dell'individuo,
cio il maggior rischio di rimanere impigliato nella dipendenza rispetto ai coetanei esposti alle stesse condizioni ambientali.

Fig. 1.
Ad essere implicati nelle sequenze causali dei disturbi da uso di sostanze sono molteplici e complessi
fattori che possono essere interpretati soltanto nel quadro di un approccio transdisciplinare.
Sempre maggiori evidenze appaiono sostenere l'ipotesi di un modello biogenetico per l'interpretazione
etiopatologica della tossicodipendenza e dell'alcoolismo.
Certamente, i meccanismi del "rinforzo" e le modalità con cui si stabilisce un comportamento condizionato
assumono un ruolo centrale tra i possibili agenti causali, pur non esaurendone l'interpretazione in modo meccanicistico.
La cascata della gratificazione
Il sistema mesolimbico con le sue componenti dell'amigdala, dell'ippocampo e
della parte ventrale del putamen, chiamata nucleus accumbens, costituisce l'apparato deputato alla percezione della gratificazione: una vera e propria
"cascata della gratificazione" coinvolge il release della serotonina che a sua volta stimola le encefaline a livello ipotalamico. L'inibizione
prodotta dalle encefaline sul GABA a livello della sostanza nigra si traduce nel release di dopamina nel nucleus accumbens. È l'accumbens che viene chiamato
"centro del piacere" e la dopamina "molecola del piacere" o "molecola antistress".
Un generale consenso della letteratura conferma che una disfunzione della cascata della gratificazione provocata da determinate varianti genetiche,
specialmente tali da provocare un vero e proprio tratto ipodopaminergico, può produrre una impercettibile condizione di malessere e una attitudine
comportamentale alla ricerca degli stimoli prodotti dalle droghe e dall'acool.
L'impairment della cascata della gratificazione può essere determinato anche a
livello recettoriale: in particolare alterazioni genetiche che coinvolgono la
struttura del recettore D2 per la dopamina sono particolarmente implicate nello sviluppo delle dipendenze.
Un comportamento addittivo, impulsivo e compulsivo connesso con carenze dei
recettori D2 viene rilevato in elevata frequenza in tutte le forme da dipendenza
da sostanze, nel binge per gli zuccheri, nel gamblimg patologico, nella sex
addiction, nel deficit di attenzione con iperattività, nella sindrome di
Tourette, nei soggetti con comportamento aggressivo persistente e nei disordini
della condotta con sviluppo di personalità antisociale.
L'insieme che conduce alla rottura della cascata della gratificazione potrebbe essere dovuto al coesistere di più polimorfismi cromosomici con alterazioni
genetiche associate a specifiche condizioni ambientali. La risultante, appunto, che viene a crearsi è il tratto ipodopaminergico che viene definito "reward
deficency syndrome", una sindrome da deficit della percezione delle gratificazioni con la necessità di stimoli sempre nuovi, fuori dall'ordinario e
a forte contenuto emozionale (Blum et at., 2000).

Fig. 2
Il sistema dopaminergico-oppioide della gratificazione è preposto a provvedere
motivazioni piacevoli ai principali "drive" del nostro comportamento, quelli che guidano verso le attività per procurarsi il cibo, quelli connessi con
l'accoppiamento e la riproduzione.
Le sostanze psicoattive da abuso si inseriscono come "gratificazioni artificiali" su questo sistema del piacere naturale insieme con le attività
a carattere compulsivo di cui abbiamo parlato poc'anzi. I comportamenti risk taking, cioè tali da esporre l'individuo a condizioni di possibile danno, sono
annoverati tra questi stimoli al di fuori della quotidianità capaci comunque di attivare il sistema della gratificazione.
Soltanto una minoranza di individui, fortunatamente, quando esposti alle condizioni ambientali tali da costituire una condizione di rischio per l'uso di
sostanze o i comportamenti compulsivi sviluppano una vera e propria dipendenza.
La tabella 1 illustra diverse condizioni che condividerebbero il tratto
ipodopaminergico di cui si è accennato nonchè la condizione comportamentale
impulsivo-addittiva-compulsiva che esprime clinicamente la sindrome da deficit
della gratificazione (Blum et al., 2000: tab. 1).

Fig. 3
Le alterazioni genetiche
Come si detto, il disturbo addittivo appare connesso dal punto di vista genetico non con una
singola alterazione neuroendocrina corrispondente ad una sola mutazione ma ad un
intreccio di polimorfiismi cromosomici capaci di agire come concause nel
determinare il livello di vulnerabilità. Un estremo rilievo è stato dato alla
presenza dell'allele 1 del gene DRD2 che codifica per il recettore D2 della
dopamina: si tratterebbe di un marker per la vulneralibità per l'alcolismo e in
contemporanea per l'antisocialità e il comportamento compulsivo, con una
alterazione della sensibilità recettoriale alla dopamina (Comings et al., 1998;Noble, 1998).

Fig. 4
Il sistema dopaminergico non appare compromesso solo a
livello recettoriale, ma anche la componente presinaptica sembra giocare un
ruolo nel determinare il tratto ipodopaminergico: una alterazione del gene che
codifica per il transporter della dopamina è stato associata alla vulnerabilitè
per le dipendenze e a più intensi sintomi astinenziali al momento della
sospensione delle sostanze (Ueno et al., 1999) (Fig. 4).
Anche il sistema della serotonina appare compromesso a partire da alterazioni
genetiche nella popolazione a rischio per lo sviluppo dei disturbi addittivi:
tra i figli degli alcolisti, e cioè in soggetti con storia familiare di
alcolismo, è stata rilevata una mutazione del gene che codifica per il
transporter della serotonina in elevata percentuale. In quest'ottica l'elevata
frequenza dell'allele S può essere addirittura interpretata con un marker
clinico e diagnostico (Nakamura et al., 1999).
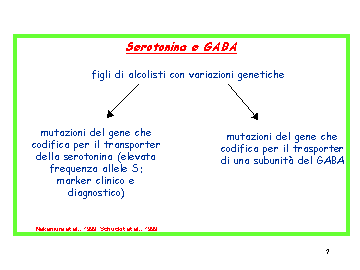
Fig. 5.
Peraltro anche il complesso macromolecolare del GABA può andare incontro ad
alterazioni funzionali che sono condizionate geneticamente, con il
coinvolgimento del transporter per il GABA stesso oppure con modificazioni delle
subunità che compongono la struttura recettoriale (Schuckit et al., 1999)(Fig. 5).
In molti modi viene coinvolto il sistema noradrenergico da mutazioni genetiche
inerenti l'alcolismo e più in generale le dipendenze. L'enzima
mono-amino-ossidasi (MAO), il principale agente del catabolismo delle
catecolamine, è codificato da un gene la cui mutazione si associa all'alcolismo
di tipo deviante e antisociale (Parsian, 1999).
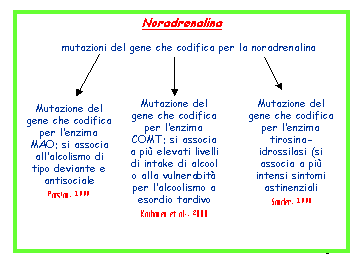
Fig. 6
Anche l'enzima COMT, controllato a partire dal patrimonio genetico, e preposto
ai meccanismi che metabolizzano le catecolamine, presenta alterazioni
conseguenti a mutazioni ed espresse con più elevati livelli di alcool-intake e
una maggiore vulnerabilità per l'alcolismo ad esordio tardivo (Kauhanen et al.,2000)(Fig. 6).
Un'altra mutazione implica alterazioni a carico dell'enzima
tirosina-idrossilasi, questa volta coinvolto nella sintesi delle catecolamine, e
si trova frequentemente associata alle forme di dipendenza da alcool con più
intensi sintomi astinenziali (Sander, 1998) (Fig. 6).
Non è escluso dalle disfunzioni provocate da fattori genetici e connesse con lo
sviluppo delle dipendenze il sistema recettoriale oppioide: alterazioni del gene
che codifica per i recettori ( sono state rilevate anche in relazione ad
alterazioni della sensibilità dopaminergica (Town et al., 1999).
Fig. 7
Si va configurando dunque un quadro complessivo che lega insieme le disfunzioni del
principale sistema della gratificazione con le alterazioni della soglia del
piacere e della analgesia.
Il quadro appare ad oggi comunque molto complesso, con dati contrastanti che non
permettono facili interpretazioni meccanicistiche: le evidenze inerenti le
alterazioni del gene che codifica per il recettore della dopamina (DRD2) non
sembrano sufficienti a supportare le condizioni di vulnerabilità per lo sviluppo
dell'alcolismo (Goldman et al., 1998).

Fig 8
|